
題目列表(包括答案和解析)
| 0.14CV |
| m |
| 14CV |
| m |
| 0.14CV |
| m |
| 14CV |
| m |
 用98%的濃H2SO4(ρ=1.84g/cm3)配制 240mL0.5mol/L的稀H2SO4,請按要求填空:
用98%的濃H2SO4(ρ=1.84g/cm3)配制 240mL0.5mol/L的稀H2SO4,請按要求填空:

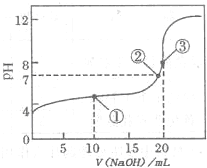 (2011?巢湖二模)滴定法是化學(xué)定量分析的一種重要而普遍的方法.
(2011?巢湖二模)滴定法是化學(xué)定量分析的一種重要而普遍的方法.| 實驗 | 樣品體積/mL | 高錳酸鉀溶液體積/mL |
| 1 | 10.00 | 8.98 |
| 2 | 10.00 | 8.58 |
| 3 | 10.00 | 9.02 |
| 4 | 10.00 | 9.00 |
| 酸 | 點解方程式 | 電離平衡常數(shù) |
| CH3COOH | CH3COOH?CH3COO-+H+ | K=1.76×10-5 |
| H2CO3 | H2CO3?HCO3-+H+ HCO3-?CO32-+H+ |
K1=4.31×10-7 K2=5.61×10-11 |
| H2S | H2S?HS-+H+ HS-?S2-+H+ |
K1=9.1×10-8 K2=1.1×10-15 |
| H3PO4 | H3PO4?H2PO4-+H+ H2PO4-?HPO42-+H+ HPO42-?PO43-+H+ |
K1=7.52×10-3 K2=6.23×10-8 K3=2.20×10-13 |
| cα2 |
| 1-α |
| cα2 |
| 1-α |
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com