
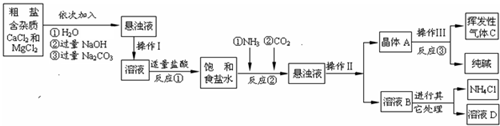
¯}─┐┴ð▒Ý(░³└¿┤░©║═¢Ô╬÷)
| ||
| ╬´┘|(zh¿¼) | NaCl | NaHCO3 | NH4Cl | NH3 | CO2 |
| ╚▄¢ÔÂ╚ | 36.0g | 9.6g | 37.2g | 710 | 0.9 |
| îì‗×Ê╗ | îì‗×Â■ | îì‗×╚² | îì‗×╦─ | |
| ╣╠¾w╗ý║¤╬´╚▄Ê║┘|(zh¿¼)┴┐ | 100g | 100g | 100g | 100g |
| ╝Ë╚ÙCaCl2╚▄Ê║┘|(zh¿¼)┴┐ | 10g | 20g | 30g | 40g |
| ╔·│╔Á─│┴ÁÝÁ─┘|(zh¿¼)┴┐ | 4g | m | 10g | 10g |
| ╣ñÿI(y¿¿)╝âëAÿ╦(bi¿ío)£╩(zh¿│n)ú║ú¿Na2CO3% ú® | |||
| â×(y¿¡u)Á╚ãÀ | Ê╗Á╚ãÀ | ║¤©±ãÀ | ┤╬ãÀ |
| í¦95 | í¦80 | í¦75 | í▄40 |

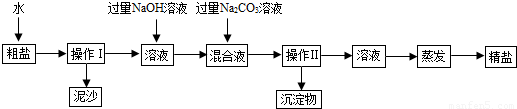


░┘Â╚Í┬ð┼ - ¥Ü┴ò(x¿¬)âÈ┴ð▒Ý - Èç¯}┴ð▒Ý
║■▒▒╩í╗Ñ┬ô(li¿ón)¥W(w¿úng)▀`À¿║═▓╗┴╝ð┼¤ó┼eê¾ã¢┼_ | ¥W(w¿úng)╔¤Ëð║ªð┼¤ó┼eê¾îúà^(q¿▒) | Ùèð┼Èp‗_┼eê¾îúà^(q¿▒) | ╔µÜv╩À╠ôƒo͸┴xËð║ªð┼¤ó┼eê¾îúà^(q¿▒) | ╔µã¾ÃÍÖÓ(qu¿ón)┼eê¾îúà^(q¿▒)
▀`À¿║═▓╗┴╝ð┼¤ó┼eê¾ÙèÈÆú║027-86699610 ┼eê¾Ó]¤õú║58377363@163.com